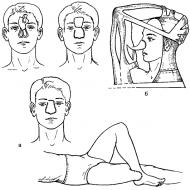
Faktorer för patogenicitet av Mycobacterium tuberculosis, deras verkningsmekanism, patogenes av tuberkulos, immunitet. Sanitär mikrobiologi Funktioner i sammansättningen av cellväggen hos tuberkulosbakterier
Tuberkulos (tuberkulos; från latin tuberculum - tuberkel) är en infektionssjukdom som orsakas av mykobakterier, kännetecknad av skador på olika organ och system (lungor, matsmältningsorgan, hud, ben, genitourinary system, etc.). Orsakas av tre typer av mykobakterier: M. tuberculosis, M. bovis, M. africanum. Alla tre arterna skiljer sig åt i morfologiska, kulturella, biokemiska och patogena egenskaper. Förutom dem inkluderar detta släkte icke-tuberkulösa eller opportunistiska mykobakterier (M. avium, M. cansasi), som ibland kan orsaka sjukdomar hos människor och djur. Patogenen upptäcktes av R. Koch (1882).
Taxonomi. Patogenen tillhör divisionen Firmicutes, familjen Mycobacteriaceae, släktet Mycobacterium.
Morfologi och färgegenskaper. Odling. M. tuberculosis - långa (1-3,5 µm), tunna (0,2-0,4 µm), lätt böjda stavar, grampositiva, orörliga, bildar inte sporer eller kapslar, färgade enligt Ziehl. På flytande media producerar de efter 2-3 veckor tillväxt i form av en skrynklig film, och på ett tätt medium bildar de en vårtaktig beläggning. Det optimala mediet för odling är äggmedium med tillsats av glycerol (Levenshtein-Jensen medium). Den optimala biologiska modellen är marsvinet. Vid mikroodling på objektglas i flytande medium bildas mikrokolonier efter 3 dagar, där virulenta mykobakterier finns i form av "flätor" eller "buntar". Detta fenomen kallas sladdfaktor. M. bovis är korta tjocka pinnar med korn. Den optimala biologiska modellen är kaniner. M. africanum är tunna, långa stavar. De växer på enkla näringsmedier. Temperaturoptimal 40,42ºС. Lågpatogen för människor. Virulenta stammar av M. tuberculosis producerar R-kolonier på fasta medier.
Enzymaktivitet. Tuberkulösa mykobakterier ger ett positivt resultat i niacintestet, minskar nitrater, sönderdelar urea, nikotinamid, pyrazinamid.
Antigen struktur. Den antigena strukturen hos mykobakterier är ganska komplex. Antigener är associerade med cellväggen, ribosomer, cytoplasman, har en protein- och lipopolysackaridnatur, deltar i reaktionerna av HRT och HNT och har skyddande aktivitet.
Motstånd. Mykobakterier är resistenta mot miljön: de kvarstår i damm i 10 dagar, på böcker och leksaker - upp till 3 månader, i vatten - upp till 5 månader, olja - upp till 10 månader, ost - upp till 8 månader, sputum - upp till 10 månader. När de kokas dör de inom 5 minuter. För desinfektion används aktiverade lösningar av kloramin och blekmedel.
Epidemiologi, patogenes och klinisk bild. Tuberkulos är utbrett och är ett socialt problem; befolkningsinfektion, sjuklighet och dödlighet är ganska hög, särskilt i underutvecklade länder. Människans mottaglighet för tuberkulos är universell. Sjukligheten påverkas av befolkningens sociala levnadsvillkor. Smittkällan är en sjuk person; Smittvägen är huvudsakligen luftburen, sällan genom hushållskontakt. Endast patienter med en öppen form av tuberkulos utgör en epidemisk fara när patogenen släpps ut i miljön. Vid infektion (inkubationstid 3,8 veckor) bildas ett primärt tuberkuloskomplex (inflammatorisk eller inflammatorisk-nekrotisk reaktion) på platsen för införandet av patogenen, vilket kan spridas och orsaka sjukdomen olika former– från mild till svår septik, med skador på olika organ och system. Oftast påverkar tuberkulos lungorna. Tuberkulosinfektion kännetecknas av en HRT-reaktion, detekterad genom intradermal injektion av tuberkulin (Mantoux-reaktion). För att utföra detta test används ett renat PPD-proteinpreparat från Mycobacterium tuberculosis. En icke-sensibiliserad organism reagerar inte på läkemedlet, men om det finns levande mykobakterier i kroppen (hos en patient eller en vaccinerad person), utvecklas en lokal inflammatorisk reaktion efter 48 timmar.
Anti-tuberkulos immunitetär ömtålig och kvarstår endast i närvaro av mykobakterier i kroppen.
Mikrobiologisk diagnostik. För laboratoriebekräftelse av diagnosen tuberkulos undersöks vanligtvis sputum, bronkialsköljvatten, urin, cerebrospinalvätska etc. Bakterioskopi av Ziehl-Neelsen-färgade utstryk är endast effektiv om det finns en hög koncentration av mykobakterier i materialet som undersöks. För att "berika" materialet som studeras, använd olika metoder i synnerhet centrifugering. Den bakteriologiska metoden, ympning på flytande och fasta näringsmedia är effektivare, men kräver 3-4 veckor. Mikroodling på objektglas i Shkolnikov-medium används som en accelererad diagnostisk metod. Ibland används en biologisk metod - infektion av ett marsvin.
Behandling. Isoniazid, rifampicin, etambutol, protionamid, pyrazinamid, cykloserin, streptomycin, kanamycin, florimycin, tioacetazon (Tibone), para-aminosalicylsyra (PAS) ordineras.
Förebyggande. Genomföra en uppsättning sanitär-hygieniska och anti-epidemiåtgärder (sanitära tillstånd för företag, barnomsorgsinstitutioner, skolor, etc., identifiering av patienter, registrering av familjer, klinisk undersökning, epidemiologisk övervakning, etc.). Specifik prevention utförs genom att administrera ett levande vaccin - BCG (Bac. Calmette. Guerin), erhållet av Calmette och Guerin genom attenuering av mykobakterier på ett speciellt medium. Nyfödda vaccineras (5-7 dagar i livet) intradermalt, följt av revaccination vid 7, 12 och 17 års ålder. Innan revaccination görs ett Mantoux-test. Om reaktionen är positiv genomförs inte omvaccination.
Morfologi av Mycobacterium tuberculosis (röda stavar) i sputum. Ziehl-Neelsen färgning. Grampositiva tunna raka eller lätt böjda stavar; - Cellväggen innehåller en stor mängd vaxer och lipider (mykolsyra), vilket bestämmer hydrofobicitet, motståndskraft mot syror, alkalier och alkoholer; - Betsad enligt Ziehl-Neelsen; - Rörlig, bildar inte sporer eller kapslar; - Kan konverteras till filtrerbara och L-former


Kulturella egenskaper Aerober; Odla på media som innehåller ägg, glycerin, potatis, asparagin, vitaminer, salter; De vanligaste är Lowenstein-Jensen äggmedium och Soton syntetiskt medium; växa långsamt (tillväxt upptäcks efter 2-3 veckor och senare); Kolonier är torra, skrynkliga, gråaktiga; De har biokemisk aktivitet som gör det möjligt att differentiera arter. Huvudtestet är niacintestet (ackumulering av nikotinsyra i ett flytande medium. Lowenstein-Jensen-medium och tillväxten av mykobakterier.


Patogenicitetsfaktorer Adhesionsfaktor - cord - faktor = ester av trehalos och rester av mykolsyra; Antifagocytiska faktorer - vaxer (särskilt vax D), sulfater och några andra föreningar som förhindrar sammansmältning av fago- och lysosomer; Sulfolipider hämmar aktiviteten av lysosomala enzymer; Fosatid- och vaxfraktioner av lipider orsakar sensibilisering av kroppen; Acetonlösliga lipider förbättrar de immunsuppressiva egenskaperna hos mykobakterier och modifierar värdcellmembran; Lipider ger resistens mot komplement och fria radikaler av fagocyter. Huvudfaktorn, tuberkulin, har toxiska och allergiska egenskaper


Interaktionen av Mycobacterium tuberculosis med människokroppen börjar när patogenen kommer in i lungorna Efter vidhäftning med hjälp av en sladdfaktor, fångas de av alveolära makrofager. Händelserna som inträffar därefter (makrofager hindrar antingen spridningen av mykobakterier eller inte) bestäms av förhållandet mellan makrofagernas bakteriedödande aktivitet och mykobakteriers virulens. Efter multiplikation inuti makrofagen, förstör mykobakterier den Monocyter, som kommer från blodomloppet under påverkan av kemotaxifaktorer, fångar mykobakterier som frigörs från förstörda makrofager, överför mykobakterier till de närmaste lymfkörtlarna, där de förblir under lång tid på grund av ofullständig fagocytos. Sålunda orsakar det initiala inträdet av patogenen i lungorna eller andra organ utveckling av mindre eller ospecifik inflammation med makrofaginfiltration.

Patogenes (fortsättning) 2-4 veckor efter infektion börjar nästa steg av interaktion mellan mykobakterier och makroorganismen. I detta fall observeras två processer - en reaktion av vävnadsskada som HRT (specifik inflammatorisk reaktion) och en reaktion av aktivering av makrofager. Med utvecklingen av immunitet och ackumulering i primärt fokus stor kvantitet aktiverade makrofager bildas ett tuberkulöst granulom Granulom består av lymfocyter och aktiverade makrofager, det vill säga epiteloida och jätteceller Utvecklingen av en vävnadsskadareaktion leder till bildandet av ett fokus av kaseös nekros. granulomet Om fokus läker blir de nekrotiska massorna tätare och förkalkade till följd av saltavsättning kalcium bildas en bindvävskapsel runt lesionen MEN mykobakterier i form av L-former behåller livskraften i en sådan lesion under många år När motståndet hos makroorganismen minskar, aktiveras fokus med utvecklingen av sekundär tuberkulos




Immunitet Anti-tuberkulos immunitet bildas som svar på penetrering av mykobakterier i kroppen under infektion eller efter vaccination och är icke-steril, smittsam till sin natur, vilket beror på långvarig persistens av L-former Den avgörande rollen tillhör till cellulär immunitet. Utfallet av sjukdomen bestäms av aktiviteten hos T-hjälpare, som aktiverar makrofagernas fagocytiska aktivitet och T-mördaraktivitet.

Epidemiologi Den huvudsakliga källan till infektion är en patient med respiratorisk tuberkulos Smittvägarna är luftburna, mer sällan matsmältningen, kontakt Mycobacterium tuberculosis är mycket stabil i den yttre miljön. I rinnande vatten de kan förbli livskraftiga i upp till 1 år, i jord och gödsel i 6 månader, på olika föremål i upp till 3 månader, i biblioteksdamm i 18 månader, i torkat pus och sputum i upp till 10 månader. När den kokas dör Kochs bacill efter 5 minuter, i magsaft efter 6 timmar, när den pastöriseras efter 30 minuter dödar direkt solljus mykobakterier inom en och en halv timme och ultravioletta strålar inom 2-3 minuter. Desinfektionsmedel som innehåller klor dödar mykobakterier inom 5 timmar.

Epidemiologi (forts.) Tuberkulos är utbredd Incidensen ökar p.g.a. socioekonomiska faktorer (den huvudsakliga faktorn är svält) Sedan 1990 har en kraftig ökning av incidensen registrerats över hela världen Humant immunbristvirus (HIV) och förvärvat immunbristsyndrom har orsakat en markant ökning av antalet fall av tuberkulos i vissa länder. problemet är spridningen av multiresistenta mykobakterier

Behandling För närvarande, enligt graden av effektivitet, är anti-tuberkulosläkemedel indelade i 3 grupper: Grupp A - isoniazid, rifampicin och deras derivat (rifabutin, rifater) Grupp B - streptomycin, kanamycin, etionamid, cykloserin, fluorokinoloner, etc. Grupp C - PAS och tioacetozon

BCG-vaccin (BCG - bacillus Calmette och Guerin) - innehåller levande avirulenta mykobakterier som erhållits från M. bovis genom långtidspassager på media som innehåller galla Immunitet efter vaccination är associerad med bildandet av överkänslighet överkänslighet (fördröjd typ överkänslighet) Specifik förebyggande

Laboratoriediagnostik Kliniskt material: pus, sputum, blod, bronkial exsudat, cerebrospinalvätska, pleuralvätska, urin etc. Metoder: 1. Bakterioskopisk: direkt färgning av ett sputumutstryk med Ziehl-Neelsen-metoden eller ett utstryk efter anrikning (koncentration med flotation eller homogeniseringsmetoder)


Laboratoriediagnostik 4. Den bakteriologiska (odlings)metoden används för att testa effektiviteten av behandlingen (2-8 veckor är nödvändiga för tillväxt av kolonier på Lowenstein-Jensen-medium och lite mer tid för att bedöma effekten av läkemedel som introduceras i tillväxtmediet ); 5. Serologisk metod (RSK, ELISA, radioimmun, etc.); 6.Biologisk metod (infektion av marsvin och kaniner med efterföljande isolering av en ren kultur av patogenen); 7. Mantoux tuberkulintest (se nedan); 8. Molekylär genetisk metod (PCR)

Mantoux hudallergitest Intradermal administrering av högrenat tuberkulin (PPD = Purified Protein Derivative) orsakar en lokal inflammatorisk reaktion i form av infiltration och rodnad (HRT-reaktion) hos personer som är infekterade med mykobakterier. Oinfekterade människor visar ingen reaktion på införandet av tuberkulin. Detta test används för att identifiera infekterade, sensibiliserade personer.

Tuberkulosbakteriers patogenicitet är förknippad med en hög lipidhalt. Ftioid-, mykol- och andra fettsyror som finns i lipider har en speciell toxisk effekt på vävnadsceller. Till exempel har fosfatidfraktionen, den mest aktiva av alla lipider, förmågan att orsaka en specifik vävnadsreaktion i en normal kropp med bildandet av epiteloidceller, och fettfraktionen - tuberkuloidvävnad. Dessa egenskaper hos dessa lipidfraktioner är förknippade med närvaron av ftioidsyra i deras sammansättning. Den vaxartade fraktionen som innehåller mykolsyra orsakar reaktioner med bildandet av många jätteceller. Således är de patogena egenskaperna hos tuberkulosbacillen och de biologiska reaktionerna som vävnaderna svarar förknippade med lipider som består av neutrala fetter, vaxer, steroler, fosfatider, sulfatider och innehåller fettsyror såsom ftioid, mykolsyra, tuberkulostearinsyra, palmitinsyra och andra. för deras genomförande. Huvudfaktorn patogenicitet är en giftig glykolipid (kabelfaktor), som finns på ytan och i tjockleken cellvägg. Förbi kemisk natur det är en polymer som består av en molekyl trehalosdisackarid och associerad med den i ekvivalenta proportioner av mykolsyra och mykolsyra högmolekylära fettsyror - trehalos-6,6"-dimikolat (C 186 H 366 Osh). Strålfaktorn har inte bara en giftig effekt på vävnad, men skyddar också tuberkulosbaciller från fagocytos, blockerar oxidativ fosforylering i makrofagernas mitokondrier, absorberas av fagocyter, de förökar sig i dem och orsakar deras död Cord-faktor har två karakteristiska egenskaper, vilket indikerar dess viktiga roll som en huvudsaklig patogenicitetsfaktor.
1. När vita möss infekteras intraperitonealt orsakar det deras död. Ingen annan del av tuberkulosbacillen har en liknande effekt.
2. Det undertrycker migrationen av leukocyter hos en person som lider av tuberkulos (in vivo och in vitro).
M. tuberculosis som saknar navelsträngsfaktorn är icke-patogen eller svagt patogen för människor och marsvin. Med det ovanliga kemisk sammansättning tuberkulosceller är också associerade med deras förmåga att orsaka en fördröjd överkänslighetsreaktion som är karakteristisk för tuberkulos, upptäckt med ett tuberkulintest.
121. Mykobakteriers egenskaper bestäms av högt lipidinnehåll.
1. Beständig mot syror, alkalier och alkohol
2. Svårt att måla med färgämnen. Intensiva metoder används för att färga dem. Till exempel, enligt Ziehl-Neelsen-metoden, färgas de med en koncentrerad lösning av karbolfuchsin vid upphettning. Blå färg, och tuberkelbaciller behåller sin ursprungliga röda färg
3. relativt hög stabilitet för torkning och exponering för solljus.
4. Beständighet mot konventionella desinfektionsmedel
5. Hög hydrofobicitet, vilket återspeglas i odlingsegenskaperna: på glycerinbuljong är tillväxten i form av en gulaktig film, som gradvis tjocknar, blir spröd och får ett ojämnt skrynkligt utseende, medan buljongen förblir transparent.
6. Patogenicitet hos tuberkulosbakterier. Ftioid-, mykol- och andra fettsyror som finns i lipider har en speciell toxisk effekt på vävnadsceller
122. Tuberkulosens epidemiologi.
Smittkällan är en person med tuberkulos (från en sjuk person frigörs patogenen oftast med sputum, såväl som med urin, avföring och pus. luftburna droppar och, särskilt ofta, luftburet damm förresten. Ingångsporten kan också vara alla slemhinnor och alla skadade områden av huden observeras oftast hos barn, eftersom mjölk fungerar som huvudfödan produkt för dem, men infektion är också möjlig från sjuka djur och aerogent. Att komma in i miljön, Mycobacterium tuberculosis länge sedan behålla sin livskraft. Således överlever de i torkat sputum i flera veckor, på föremål som omger patienten (linne, böcker) i mer än 3 månader, i vatten i mer än ett år, i jord i upp till 6 månader och bevaras under lång tid i mejeriprodukter. Till verkan av desinfektionsmedel
GBOU VPO "Ural State Medical University" vid hälsoministeriet Ryska Federationen Institutionen för mikrobiologi, virologi och immunologi
Riktlinjer för praktiska övningar för studenter
OOP specialitet 060301.65 Apoteksdisciplin C2.B.11 Mikrobiologi
1. Ämne: Tuberkulospatogener
2. Lektionens mål: Att tillsammans med eleverna studera tuberkulospatogeners egenskaper, patogenicitetsfaktorer, patogenes, metoder för diagnostik, förebyggande och behandling av tuberkulos.
3. Mål för lektionen:
3.1. Studera egenskaperna hos tuberkulospatogener.
3.2. Studie av patogenesen av tuberkulos.
3.3. Studie av metoder för diagnos, förebyggande och behandling av tuberkulos.
3.4. Gör självständigt arbete.
kompetens |
||||
Förmåga och |
Morfologiska |
njut av |
Färgningsteknik |
|
beredskap |
ledtrådar, kulturella |
verktyg |
läkemedel enligt Tsil- |
|
analysera |
ny, biokemi- |
när man genomför |
Nielsen |
|
socialt betydelsefulla |
kemiska egenskaper |
mikrobiologiska |
||
problem och processer, |
patogener |
forskning |
||
använda på |
tuberkulos |
|||
öva metoder |
||||
humanitär, |
||||
naturvetenskap, |
||||
biomedicinska |
||||
och klinisk vetenskap inom |
||||
professionella och |
||||
social |
||||
aktiviteter |
||||
Förmåga och |
Principer och |
Uppträdande |
||
vilja att delta |
sanitär |
biologisk |
||
vid inrättandet av vetenskapliga |
diagnostik |
pedagogisk |
konceptuella |
|
uppgifter och deras |
förebyggande och |
arbeta med befolkningen |
anordning |
|
experimentell |
||||
genomförande |
tuberkulos |
4. Lektionens längd i akademiska timmar: 3 timmar.
5. Säkerhetsfrågor om ämnet:
5.1. Morfologiska, tinktoriella, kulturella och biokemiska egenskaper hos tuberkulospatogener.
5.2. Patogenicitetsfaktorer för tuberkulospatogener.
5.3. Metoder för diagnos, förebyggande och behandling av tuberkulos.
6. Uppgifter och riktlinjer för deras genomförande.
Under lektionen ska eleven:
6.1. Svara på lärarens frågor.
6.2. Delta i diskussionen om de frågor som studeras.
6.3. Gör självständigt arbete.
Teoretisk information Tuberkulos- kronisk infektion, åtföljs
specifika skador på olika organ och system (andningsorgan, lymfkörtlar, tarmar, skelett, leder, ögon, hud, njurar, urinvägar, könsorgan, centrala nervsystemet). Med tuberkulos bildas specifika granulom (granulum - korn) i organ i form av knölar eller tuberkler (tuberkulum - tuberkel), följt av deras curdled degeneration (sönderfall) och förkalkning.
Historisk referens. MED antiken denna sjukdom var känd under namnen konsumtion, tuberkel, scrofula på grund av dess karakteristiska kliniska tecken. Laennec var den första som skilde "konsumtion" från andra lungsjukdomar 1819, han myntade termen "tuberkulos" (därav synonymen - tuberkulos). År 1882 upptäckte R. Koch det orsakande medlet av tuberkulos och erhöll en ren kultur på ett serummedium (Kochs bacill eller bacillus). År 1890 erhöll R. Koch tuberkulin ("vatten-glycerolextrakt från tuberkuloskulturer"). 1911 tilldelades R. Koch Nobelpriset för upptäckten av tuberkulosens orsaksämne.
Taxonomi. Division Firmicutes, familjen Mycobacteriaceae, släktet Mycobacterium.
Tuberkulos hos människor orsakar oftast tre typer av mykobakterier: M. tuberculosis (Kochs bacillus, mänsklig art - orsakar sjukdom i 92% av fallen), M. bovis (nötkreatur - orsakar sjukdom i 5% av fallen), M. africanum (mellanart - orsakar sjukdom i 3 % av fallen, mycket vanligare i Sydafrika). I sällsynta fall orsakas tuberkulos hos människor av M. microti (mustyp) och M. avium (fågeltyp, som orsakar infektion hos immunförsvagade individer).
Morfologiska och tinktoriella egenskaper. De orsakande medlen för tuberkulos kännetecknas av uttalad polymorfism (coccoid, filamentös, grenad, kolvformade former). De har huvudsakligen formen av långa tunna ( M. tuberculosis, M. africanum ) eller kort och tjock ( M. bovis ) stavar med granulär cytoplasma innehållande från 2 till 12 korn olika storlekar(korn av metafosfater - Mukha-korn). Ibland bildar de trådliknande strukturer som påminner om svampmycel, vilket är grunden för deras namn ( mykes - svamp och bakterie - bakterie). Fast. Det finns ingen tvist. De har en mikrokapsel.
Gram positiv. Mykobakterier är syra-, alkohol- och alkaliresistenta bakterier. För deras färgning används Tsil-metoden.
Nielsen (termisk syraetsning med karbolfuchsin). Med denna färg ser mykobakterier ut som ljusröda stavar, placerade ensamma eller i små kluster av 2-3 celler.
Kulturfastigheter. Obligatorisk aerob. De växer långsamt på grund av förekomsten av lipider i cellväggen, som bromsar ämnesomsättningen med omgivningen. Optimal temperatur tillväxt 37-38ºС. Det optimala pH-värdet är 6,8-7,2. Mykobakterier kräver näringsmedier, glycerolberoende. För att undertrycka den toxiska effekten av fettsyror som bildas under ämnesomsättningen tillsätts aktivt kol, animaliskt blodserum och albumin till mediet, och för att undertrycka tillväxten av medföljande mikroflora tillsätts färgämnen (malakitgrönt) och antibiotika som inte verkar på mykobakterier. .
Valbar kulturmedia för mykobakterier:
Äggmedia Levenshtein-Jensen, Finn-2;
- Middlebrook glycerol media;
- potatismedia med galla;
- halvsyntetiskt medium Shkolnikova;
- syntetiska media Soton, Dubos.
På fasta medier, på inkubationsdagarna 15-20, bildar mykobakterier grova, täta, krämfärgade, vårtaktiga kolonier (som påminner om
blomkål).
I flytande media bildas efter 5-7 dagar en tjock, torr, skrynklig, krämfärgad film på ytan. Samtidigt förblir buljongen genomskinlig.
För expressdiagnostik används metoden för mikroodling på glasögon i ett flytande medium ( Pris mikrokultur metod), där tillväxten av mykobakterier efter 48-72 timmar noteras i form av sammanflätade flickaktiga "flätor" eller "selar" på grund av sladdfaktorn (engelsk sladd - tourniquet, rep).
Kemisk sammansättning. Huvudkomponenterna i mykobakterier: proteiner (tuberkuloproteiner), kolhydrater och lipider.
Tuberkuloproteiner utgör 56 % av den torra massan av mikrobiellt cellmaterial. De är de huvudsakliga bärarna av mykobakteriers antigena egenskaper, är mycket giftiga och orsakar utvecklingen av typ 4-överkänslighetsreaktioner.
Polysackarider står för 15 % av den torra massan av mykobakterier. Dessa är släktspecifika haptener.
Andelen lipider (ftionsyra, smörsyra, palmitinsyra, tuberkulostearinsyra och andra fettsyror, navelsträngsfaktor och vax D, som inkluderar mykolsyra) står för 10 till 40 % av den mykobakteriella substansens torrmassa. Den höga lipidhalten bestämmer patogenens syra-, alkohol- och alkaliresistens, virulens, svårigheter att färga celler med konventionella metoder och stabilitet i miljön. Lipider skyddar bakteriecellen, undertrycker fagocytos, blockerar aktiviteten hos cellulära enzymer och orsakar utveckling av granulom och kaseös nekros.
Motstånd. I det torkade sputumet hos en patient förblir cellerna livskraftiga och virulenta i 5-6 månader. De förblir på patientens föremål i mer än 3 månader. De förblir i jorden i upp till 6 månader, i vatten i upp till 15 månader. solljus orsakar mykobakteriers död på 1,5 timmar, UFL – på 2-3 minuter. Under pastörisering dör de inom 30 minuter. Klorinnehållande
drogerna orsakar tuberkulospatogeners död inom 3-5 timmar, 5% fenollösning - efter 6 timmar.
Faktorer för patogenicitet hos mykobakterier:
Cord factor är en cellväggsglykolipid som orsakar skador på cellmembranen och hämmar bildandet av fagolysosomer, vilket orsakar utvecklingen av ofullständig fagocytos;
Lipider som innehåller mykol- och ftionsyror orsakar uppkomsten av många jätteceller;
De orsakande medlen för tuberkulos producerar inte exotoxiner. Cellnedbrytningsprodukter är mycket giftiga.
Huvudfaktorn i mykobakteriers patogenicitet är sladdfaktorn (namnet kommer från engelska sladden - tourniquet, rep). Sladdfaktorn bestämmer den "trängda typen av tillväxt" i flytande media i form av "tvinnade strängar" (eller flätor), där mykobakteriella celler är ordnade i parallella kedjor.
Epidemiologi. Tuberkulos är utbredd. Den huvudsakliga smittkällan är en sjuk person med respiratorisk tuberkulos, släpper ut mikrober i miljön med sputum. Smittkällor kan också vara personer med extrapulmonella former av tuberkulos och sjuka djur (nötkreatur, kameler, grisar, getter och får). Huvudmekanismen för infektion– aerogen. Vägar för överföring av patogenen - luftburet Och luftburet damm. Ingångsportarna är slemhinnan i munhålan, bronkerna och lungorna. Mindre vanligt kan infektion med tuberkulos uppstå via matsmältningsvägen genom konsumtion av termiskt obearbetat kött och mejeriprodukter. Tillgängliga kontakt-hushåll vägen för överföring av infektion från tuberkulospatienter genom användning av infekterade kläder, leksaker, böcker, disk och andra föremål. Det finns kända fall av mänsklig infektion när man tar hand om sjuka djur.
Patogenes. Efter att ha penetrerat människokroppen fagocyteras mykobakterier.
I I fagocyter bildas fagosomer, inuti vilka mykobakterier förblir vid liv och förökar sig. I fagocyter transporteras mykobakterier till regionala lymfkörtlar och förblir under lång tid i ett "vilande" tillstånd (ofullständig fagocytos). Detta orsakar inflammation i lymfsystemet ( lymfangit) och lymfkörtlar (lymfadenit). På platsen för patogenpenetration bildas ett fokus för inflammation. Under loppet av flera veckor blir denna inflammation specifik (en fördröjd överkänslighetsreaktion utvecklas), vilket resulterar i bildandet av ett granulom. Därefter omvandlas makrofager till epiteloidceller. När epiteloidceller smälter samman bildas gigantiska flerkärniga celler. En bindvävskapsel bildas runt källan till inflammation, och nekrotiska vävnader förkalkas. Som ett resultat av detta sker bildningen primärt tuberkuloskomplex, inuti vilken det finns kaseös nekrotisk vävnad och levande mykobakterier finns kvar.
Klinik. Inkubationsperiod varar från 3-8 veckor till 1 år eller mer.
De kliniska manifestationerna av tuberkulos varierar, eftersom mykobakterier kan påverka alla organ (tarm, genitourinära organ, hud, leder). Symtom på tuberkulos är trötthet, svaghet, viktminskning
kropp, långvarig låggradig feber, rikliga nattliga svettningar, hosta med blodig sputum, andnöd. Det finns inga symtom som är unika för tuberkulos. När huden är skadad noteras ulcerösa lesioner. Med tuberkulos i ben och leder uppstår lesioner som är karakteristiska för artrit av vilken etiologi som helst: förtunning av brosk, utseende av ryggar, förträngning av ledhåligheter.
Immunitet. Anti-tuberkulos immunitet bildas som svar på penetration av mykobakterier i kroppen under infektion eller vaccination och är icke-steril till sin natur, vilket beror på långvarig beständighet av bakterier i kroppen. Det visar sig 4-8 veckor efter att mikrober kommit in i kroppen. Både cellulär och humoral immunitet bildas.
Cellulär immunitet yttrar sig som ett tillstånd av ökad känslighet (sensibilisering). Tack vare detta förvärvar kroppen förmågan att snabbt binda en ny dos av patogenen och ta bort den från kroppen: T-lymfocyter känner igen celler infekterade med mykobakterier, attackerar dem och förstör dem.
Humoral immunitet manifesteras av syntesen av antikroppar mot mykobakteriella antigener. Cirkulerande immunkomplex (CIC) bildas, som hjälper till att avlägsna antigener från kroppen.
Immuniteten mot tuberkulos varar så länge som patogenen finns i kroppen. Sådan immunitet kallas icke-steril eller smittsam. Efter att kroppen har befriats från mykobakterier försvinner immuniteten snabbt.
Mikrobiologisk diagnostik. Materialet som testas är sputum,
bronkial aspirat, fistel flytningar, CSF, urin, avföring. Oftast undersöks sputum. Grundläggande och ytterligare forskningsmetoder används för att diagnostisera tuberkulos.
Grundläggande metoder:
- bakterioskopisk metod (ljus- och fluorescensmikroskopi);
- bakteriologisk metod.
Ytterligare metoder:
- biologisk metod;
- serologisk metod;
- hudallergitester;
- molekylärbiologi metod (PCR).
Bakterioskopisk undersökning – detta är upprepad direktmikroskopi av utstryk från testmaterialet, färgat enligt Ziehl-Neelsen. Enstaka mikroorganismer kan påvisas i preparat om 1 ml sputum innehåller minst 10000-100000 bakterieceller (metodgräns). Denna metod tillämpas:
- vid undersökning av personer med symtom misstänkta för tuberkulos (hosta med sputumproduktion i mer än 3 veckor, bröstsmärtor, hemoptys, viktminskning);
- hos personer som har varit i kontakt med tuberkulospatienter;
- hos personer med röntgenförändringar i lungorna misstänkta för tuberkulos.
Om negativa resultat erhålls, tillgriper de metoder för materialberikning: centrifugering(sedimentation) och flotation. Flotationsmetoden används oftast.
Centrifugeringsmetod– testmaterialet behandlas med alkali och centrifugeras. Ett preparat för mikroskopi framställs från sedimentet.
Flotationsmetod - materialet som studeras behandlas med en blandning av alkali och xylen (bensin, bensen, toluen). Provet skakas kraftigt i 10-15 minuter, destillerat vatten tillsätts och hålls i 1-2 timmar vid rumstemperatur. Kolhydratdroppar adsorberar mykobakterier och flyter upp till ytan och bildar skum på ytan. Ett preparat för mikroskopi framställs av det resulterande skummet.
Bakteriologisk forskning utförs genom att så testmaterialet (efter behandling med en 6-12% svavelsyralösning) på 2-3 näringsmedier av olika sammansättning samtidigt. Som accelererade metoder för bakteriologisk diagnostik, för att minska tiden för isolering och identifiering av patogenen till 3-4 dagar, är mikrokulturmetoden (Price-metoden), såväl som helautomatiserade kommersiella buljongodlingssystem VASTES MGIT 960 och MV/VasT. Begagnade.
Den bakteriologiska metoden gör att man kan erhålla en renkultur att bestämma dess virulens och känslighet för mediciner. Denna metod används i stor utsträckning för att övervaka behandlingens effektivitet.
Biologiskt provär den mest känsliga, eftersom den låter dig upptäcka från 1 till 5 mikrobiella celler i testmaterialet. Metoden används vid undersökning av biopsimaterial, samt när negativa resultat erhålls med de två första forskningsmetoderna. För att göra detta injiceras marsvin subkutant eller intraperitonealt med testmaterialet (1 ml). Efter 1-2 månader utvecklar djuren generaliserad tuberkulos med dödlig utgång.
Serologisk metod. Föreslagen av RSK, RNGA, kopplad immunosorbentanalys, immunoblotting, bestämning av CEC.
Tuberkulindiagnostik bygger på att bestämma kroppens ökade känslighet för tuberkulin (som ett resultat av infektion med tuberkulospatogener eller specifik vaccination) med hjälp av hudallergitester. Tuberkulin används för att utföra ett hudallergitest. Tuberkulin är det allmänna namnet för läkemedel erhållna från mänskliga eller bovina mykobakterier:
- gammalt Koch tuberkulin - ATK (Alt Tuberculin Koch), först erhållen 1880 av R. Koch. Det är ett filtrat av en autoklaverad 5-6 veckors buljongkultur av Mycobacterium tuberculosis;
- torr renat tuberkulin - PPD (Purified Protein Derivative),
erhållna från kulturer av M. tuberculosis och M. bovis;
- renat tuberkulin framställt av M.A. Linnikova(PPD-L) från kulturer av M. tuberculosis och M. bovis.
För att diagnostisera tuberkulos användes från början Pirquet-hudtestet (markbildningstest). För närvarande, för att snabbt identifiera
primär infektion hos barn och ungdomar används intradermalt Mantoux-test. När Mantoux-testet utförs, injiceras tuberkulin (PPD) strikt intradermalt på den inre ytan av den mellersta tredjedelen av underarmen tills en "knapp" bildas. Testresultaten beaktas efter 48-72 timmar baserat på närvaron av en papel. Mantoux-testet utvärderas enligt följande:
- negativ - närvaron av en reaktion från en injektion upp till 2 mm i diameter;
- tveksamt - papulediameter 2-4 mm eller hyperemi;
- positiv - papulediameter 5-17 mm hos barn och ungdomar och 5-21 mm
hos vuxna;
- hyperergisk - en papel med en diameter på mer än 17 mm hos barn och ungdomar och mer än 21 mm hos vuxna.
Tuberkulinreaktionen blir positiv 4-6 veckor efter infektion eller vaccination. Efter vaccination kvarstår positiva reaktioner på tuberkulin i 3-7 år. Ett positivt resultat bör inte ses som ett tecken på en aktiv process. Ett positivt Mantoux-test indikerar att en person tidigare har smittats med mykobakterier. Personer med positiva tuberkulintester löper risk för sjukdom till följd av aktivering av det primära fokuset. Om en positiv reaktion hos vuxna indikerar infektion, hos barn som inte tidigare har svarat på tuberkulin, uppträder en första registrerad positiv reaktion ( tuberkulinprovsväng) indikerar nyligen genomförd infektion och fungerar som en indikation för klinisk undersökning och behandling.
Om reaktionen är negativ finns ingen risk för aktivering av primärfokus, men det finns risk för primär infektion. Ett negativt test observeras hos friska oinfekterade individer, såväl som hos patienter med mellanliggande former av tuberkulos.
För uttrycklig diagnostik tuberkulos, RIF används med artspecifika monoklonala antikroppar, laserfluorescensmetod, mikrobiochips, samt PCR, vilket kan minska forskningen till 2 dagar.
Behandling. Antibiotikabehandling är den huvudsakliga metoden för behandling av tuberkulos. Beroende på graden av effektivitet är anti-tuberkulosläkemedel indelade i 3 grupper:
Grupp A - mest effektiva läkemedel: isoniazid (en antimetabolit, en analog av isonicotinsyra, hämmar syntesen av enzymer involverade i syntesen av mykolsyror, som är en del av mykobakteriers cellvägg), rifampicin och deras derivat. Läkemedel som är överlägsna rifampicin har erhållits medicinska egenskaper(rifapentin och rifabutin), såväl som kombinationsläkemedel (rifater, rifang, etc.);
Grupp B - medeleffektiva läkemedel: etambutol (syntetiskt läkemedel, hämmar enzymer involverade i syntesen av cellväggen hos mykobakterier, är endast aktiv mot reproducerande bakterier), kanamycin, streptomycin, cykloserin, etionamid (protionamid), pyrazinamid, florinolon, fluorokinolon derivat;
Grupp C - små läkemedel mot tuberkulos (PAS och Tibon eller Thiocetozon). Denna grupp av läkemedel används inte i ekonomiskt utvecklade länder och i Ryssland.
Stammar av mykobakterier som är resistenta mot anti-tuberkulosläkemedel uppträder mycket snabbt. Därför används kombinationer av läkemedel med olika verkningsmekanismer och läkemedel ersätts också ofta. Detta bromsar uppkomsten av resistenta former. I moderna behandlingsregimer används 3-5 läkemedel samtidigt (tre- till femkomponents behandlingsregimer).
Specifik förebyggande. Specifik prevention utförs genom att administrera ett levande BCG-vaccin (BCG - Bacille Calmette-Guerin). BCG-stammen valdes 1919 av A. Calmette och C. Guerin genom långvarig passage M. bovis på potatis-glycerinmiljö med tillsats av galla.
Vaccination utförs hos nyfödda den 3-7:e levnadsdagen intradermalt. Ett infiltrat med en liten knöl i mitten bildas på platsen för vaccinadministrering. Omvänd utveckling av infiltratet sker inom 3-5 månader. Revaccination utförs vid 7 och 14 års ålder för personer med en negativ Mantoux-reaktion, därför görs ett Mantoux-test innan det. Hos nyfödda med nedsatt resistens och i regioner fria från tuberkulos används det mindre reaktogena BCG-M-vaccinet som innehåller 2 gånger färre mikrober.
Efter diskussion För teoretiska frågor förklarar läraren proceduren för att utföra självständigt arbete.
Självständigt arbete:
1. Eleverna förbereder preparat från kulturer av icke-patogena mykobakterier, färgar dem enl Ziehl-Neelsen, mikroskopi, skissa en mikroskopisk bild i en arbetsbok.
2. I arbetsbok eleverna skissar ett diagram över laboratoriediagnostik av tuberkulos.
7. Bedömning av kunskaper, färdigheter och förmågor om ämnet för lektionen:
Svar på frågor och aktivitet i klassen bedöms enligt ett 5-poängssystem.
8. Litteratur för att förbereda ämnet:
8.1. Huvudsakliga:
1. Galynkin V., Zaikina N., Kocherovets V. Fundamentals of pharmaceutical microbiology. 2008.
2. Medicinsk mikrobiologi, virologi och immunologi: en lärobok för läkarstudenter. Ed. A.A. Vorobyova. Läroböcker och läroböcker hjälpmedel för högre utbildning. Utgivare: Medicinsk informationscentral, 2012. – 702 sid.
3. Mikrobiologi: lärobok. för studenter vid högre lärosäten. prof. utbildning, elever inom specialiteten 060301.65 ”Apotek” / red. V.V. Zvereva, M.N. Boychenko. – M.: GEOTAR-Media, 2012. – 608 s.: ill.
4. Odegova T.F., Oleshko G.I., Novikova V.V. Mikrobiologi. Lärobok för farmaceutiska universitet och fakulteter. - Perm, 2009. - 378 sid.
8.2. Ytterligare:
1. Korotyaev A.I. Medicinsk mikrobiologi, immunologi och virologi: Lärobok för läkarstudenter. universitet / A.I. Korotyaev, S.A. Babichev. - 5:e uppl., rev. Och
Lägg till. – St Petersburg: SpetsLit, 2012. – 759 s.: ill.
2. Medicinsk mikrobiologi: lärobok. 4:e uppl. Pozdeev O.K. / Ed. IN OCH. Pokrovsky. – 2010. – 768 sid.
3. Manual för medicinsk mikrobiologi. Allmän och sanitär mikrobiologi. Bok 1 / Coll. författare // Redigerad av Labinskaya A.S., Volina E.G. – M.: BINOM Publishing House, 2008. – 1080 s.: ill.
Riktlinjerna har reviderats och kompletterats av professor N.V. Litusov.
Diskuterades vid ett möte på institutionen för mikrobiologi, virologi och immunologi.
Mycobacterium tuberculosis (MBT) tillhör bakteriefamiljen Mycobacteriaceae, i ordning Actinomycetalis, familj Mycobacterium. Släkte Mycobacterium har över 100 arter, varav de flesta är saprofytiska mikroorganismer som är utbredda i miljön.
Etymologiskt kommer ordet "mykobakterier" från de grekiska orden mycer - svamp och bakterie, baktron - pinne, kvist. Namnets "svamp"-komponent kommer från dessa mikroorganismers tendens att bilda filamentösa och förgrenade mögelliknande former.
Ur klinisk medicins synvinkel är Mycobacterium tuberculosis, upptäckt av den tyske forskaren Robert Koch, den viktigaste typen av aktinomyceter, som är förenade i ett komplex bl.a. M.tuberkulos(MBT); M.bovis och dess variant BCG (Bacillus Calmette-Guerin); M.africanumdem.mikroti. Denna grupp av mykobakterier kännetecknas av uttalad genetisk likhet.
M.mikroti anses icke-patogent för människor, men orsakar en sjukdom hos möss som liknar tuberkulos. BCG-odling är inte patogen för människor. Mycobacterium tuberculosis (MBT) är orsaken till human tuberkulos i upp till 95% av fallen, beroende på bostadsområde. På samma gång M.bovis Och M.africanum orsaka en sjukdom hos människor som kliniskt inte skiljer sig från klassisk tuberkulos.
Mykobakterier ingår inte i komplexet M.Tuberkulos, kan orsaka mykobakterios. Sådana mykobakterier kombineras till komplex, av vilka de viktigaste är: M.avium, M.fortinatum Och M.terrae, M.leprae, M.sår.
Materialen som presenteras nedan om tuberkulos avser endast sjukdomen som orsakas av M.tuberkulos(MBT), - Koch-bakterier (KB), typus humanus.
Den naturliga reservoaren av mycobacterium tuberculosis är människor, tama och vilda djur och fåglar.
MBT är externt tunna, böjda pinnar som är resistenta mot syror, alkalier och torkning. Bakteriens yttre skal innehåller komplexa vaxer och glykolipider.
MBT kan föröka sig både i makrofager och utanför celler.
MBT reproducerar sig relativt långsamt. Reproduktion sker huvudsakligen genom enkel celldelning. På berikade näringsmedier multiplicerar MBT med en fördubblingstid på 18 till 24 timmar. För tillväxt i odling av Mycobacterium tuberculosis erhållen under kliniska förhållanden, tar det 4 till 6 veckor.
MBTs har ingen oberoende rörelse. Temperaturgränserna för tillväxt är mellan 29 och 42 ° C (optimalt - 37-38 °C). MBT är resistenta mot fysikaliska och kemiska ämnen; de förblir livskraftiga vid mycket låga temperaturer och tål höjningar till 80°C i 5 minuter.
I den yttre miljön är Mycobacterium tuberculosis ganska stabil. Den kan överleva i vatten i upp till 150 dagar. Torkade mykobakterier orsakar tuberkulos hos marsvin efter 1-1,5 år, lyofiliserade och frysta är livskraftiga i upp till 30 år.
I intensiv solexponering och höga temperaturer miljö kontorets lönsamhet minskar kraftigt; tvärtom, i mörker och fukt är deras överlevnadsgrad mycket betydande. Utanför en levande organism förblir de livskraftiga i många månader, särskilt i mörka, fuktiga rum.
MBT upptäcks av en unik färgningsegenskap (syrafasthet), som skiljer dem från många andra smittämnen. Ziehl och Neelsen utvecklade 1883 en speciell kontrastmetod för färgning av MBT, baserad på egenskapen syrabeständighet. Preparatet, färgat genom upphettning med karbolfuchsin, avfärgas med en lösning av svavelsyra och färgas efter tvätt med vatten med en lösning av metylenblått (Ziehl-Neelsen-metoden). Till skillnad från icke syrafasta bakterier färgas tuberkulösa mykobakterier röda, missfärgas inte när de utsätts för en sur lösning och är tydligt synliga mot blå bakgrund under mikroskopi. Ziehl-Neelsen-metoden är fortfarande en av huvudmetoderna för färgning av MBT under mikroskopi. Mer känslig än den syrafasta färgningsmetoden är MBT-auraminfärgning följt av fluorescensmikroskopi (Fig. 1-1-1, 1-1-2, se infällning).
Lipidfraktionen av det yttre skalet av MBT är associerad med resistensen hos tuberkulospatogener mot syror, alkalier och alkoholer.
Variabilitet av MBT-morfologi
Kontorets morfologi och storlek är inte konstanta det beror på cellernas ålder och särskilt på näringsmediets levnadsförhållanden och sammansättning.
Sladdfaktor.
Lipider i mykobakteriers ytvägg bestämmer dess virulens och förmåga att bilda kluster av bakterier i kulturen i form av flätor (cord factor).
Sladdfaktorn nämndes redan av Koch i hans första meddelande angående MBT. Inledningsvis associerades sladdfaktorn med virulensen hos MBT. Förmågan att bilda flätor observeras bland andra mykobakterier som har låg eller ingen virulens. Sladdfaktorn visade sig senare vara associerad med en ovanlig biologisk substans, trehalos 6,6-dimykolat, som är mycket virulent.
L-former.
En av viktiga arter Variabiliteten hos MBT är bildandet av L-former. L-former kännetecknas av en minskad nivå av ämnesomsättning och försvagad virulens. Om de förblir livskraftiga kan de stanna kvar i kroppen under lång tid och inducera immunitet mot tuberkulos.
L-former kännetecknas av uttalade funktionella och morfologiska förändringar. Det visade sig att omvandlingen av MBT till L-former ökar med långvarig exponering för antibakteriell terapi och andra faktorer som stör deras tillväxt och reproduktion, och bildandet av cellmembranet.
Det har fastställts att sputum från "abacillära" patienter med destruktiva former av tuberkulos kan innehålla L- former av MBT som under lämpliga förhållanden kan vända (modifieras) till en stavformad variant och därigenom orsaka reaktivering av tuberkulosprocessen. Följaktligen betyder abacillation av håligheterna hos sådana patienter ännu inte deras sterilisering med avseende på MBT.
MBT är i sig okänsligt för många antibiotika. Denna egenskap beror främst på det faktum att den mycket hydrofoba cellytan fungerar som en slags fysisk barriär mot terapeutiska medel och antibiotika. främsta orsaken resistens kodas i genomstrukturen hos tuberkulosbacillen.
Samtidigt kan ILO:er utveckla resistens (resistens) mot läkemedel mot tuberkulos. Samtidig läkemedelsresistens av MBT mot flera läkemedel i senaste åren avsevärt minskar effektiviteten av tuberkulosbehandling.
Som ett resultat av detta sysslar modern sjukvård med mer än bara farlig patogen tuberkulos, men med en hel uppsättning av dess stammar, resistent mot olika läkemedel. I praktiken för organisationen effektiv behandling tuberkulos, är det viktigt att inte bara upptäcka MBT, utan också att samtidigt bestämma deras resistens, och tillräckligt snabbt - inom två till tre dagar, för att ordinera effektiv kemoterapi i tid.
I slutet av 80-talet. Under det senaste århundradet har en metod dykt upp som avsevärt minskar tiden för sådan analys. Ny diagnostik baseras på selektiv amplifiering av nukleinsyror (DNA eller RNA) i vitroMed med användning av polymeraskedjereaktion (PCR).
PCR-metoden har stor potential och ligger till grund för exakt DNA-diagnostik, vilket gör att man kan identifiera vilken MBT-stam som helst och fastställa grundorsaken till en viss läkemedelsresistens.
Laboratoriestudier har visat att uppkomsten av resistens i M.tuberkulos associerade med nukleotidsubstitutioner (mutationer) i gener som kodar för olika enzymer som direkt interagerar med läkemedel.